Em certo momento da história humana, pesquisadores que estudavam ciências sentiram a necessidade de organizar os elementos químicos e fornecer o máximo possível de informações sobre eles para facilitar a consulta. A partir disso, vários cientistas tentaram e propuseram propostas diferentes para esta organização. E foi assim que surgiu a famosa Tabela Periódica! Mas você sabe o que é isso e para que serve? Veja no texto a seguir!
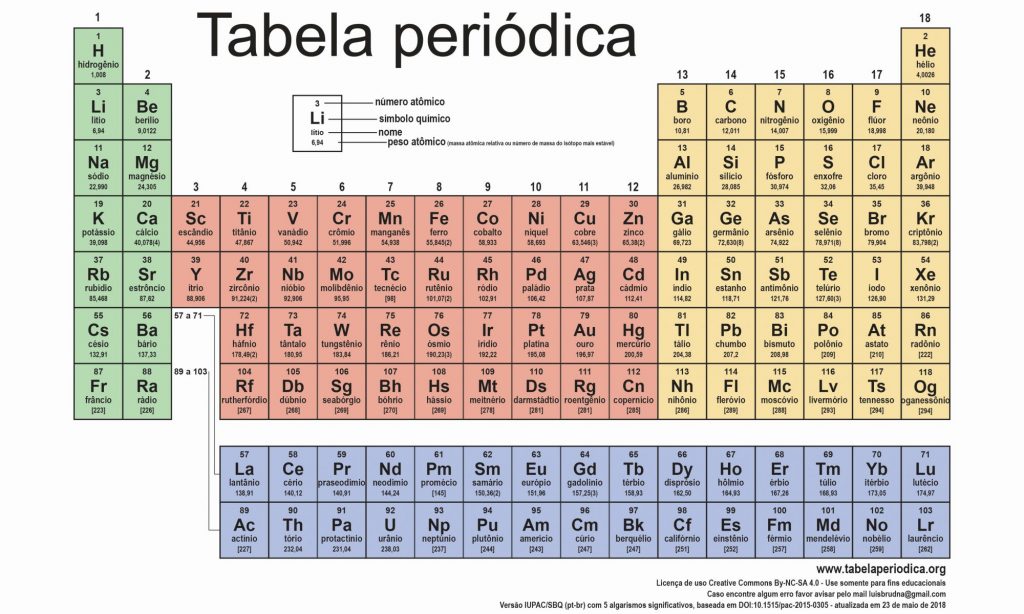
O que é Tabela Periódica?
Tabela Periódica é um modelo gráfico de uma organização sistemática que agrupa elementos químicos existentes na Terra com base em seus números atômicos (número de prótons), configurações eletrônicas e propriedades periódicas. Ele foi criado pelo físico-químico britânico Henry Moseley, em 1913. Na época, ele investigava como os elementos químicos se repetem periodicamente ao serem postos em ordem crescente de seus números atômicos. No total, são 118 elementos químicos, dos quais 92 são naturais e 26 artificiais.

A saber, este padrão é recomendado pela União Internacional de Química Pura e Aplicada (IUPAC). Há também a Tabela de Mendeleev, do químico russo Dmitri Mendeleev, do ano de 1869, mas sua versão original foi perdida. Contudo, esta sua tabela foi sendo aprimorada ao longo dos anos até sua forma atual!
Como é a Tabela Periódica hoje?
A Tabela Periódica é dividida em vários quadradinhos com os símbolos dos elementos químicos – nome e número atômico -, aproximados conforme a lógica de organização proposta pelos cientistas. São 18 colunas verticais, chamadas de grupos ou famílias – divididas em famílias A ou famílias B, sendo A a família dos elementos representativos e B a família dos elementos de transição; ou seja, elementos com propriedades físico-químicas semelhantes. Depois, sete colunas horizontais, conhecidas como períodos – que indicam a quantidade de níveis de energia presentes em cada átomo de cada elemento químico.
Dentro da Tabela, os elementos químicos são colocados em ordem crescente de número atômico. Há várias subdivisões internas, diferenciando os elementos em metal ou ametal, representativos ou de transição, além de subdividi-los de acordo com sua distribuição eletrônica – camadas K e L, e assim por diante.
Família dos elementos químicos
São famílias de elementos químicos:
PUBLICIDADE
CONTINUE LENDO ABAIXO
- Família 1: Metais Alcalinos (lítio, sódio, potássio, rubídio, césio e frâncio);
- 2: Metais Alcalinos Terrosos (berílio, magnésio, cálcio, estrôncio, bário e rádio);
- 16: Calcogênios (oxigênio, enxofre, selênio, telúrio, polônio e livermório);
- 17: Halogênios (flúor, cloro, bromo, iodo, astato e tenessino); e
- 18: Gases Nobres (hélio, neônio, argônio, criptônio, xenônio, radônio e oganessônio).
Quais as outras classificações para elementos químicos?
Os elementos químicos podem ser classificados em semimetais e metais (em branco na tabela), ametais (azul), gases nobres e hidrogênio (amarelo), segundo a sua natureza (verdes) – aliás, o hidrogênio é o elemento mais abundante de todo o universo e o quarto elemento mais abundante no planeta Terra. Também podemos separar os elementos por estados físicos – líquidos, gasosos e sólidos. E, por fim, naturais ou artificiais, produzidos pelo homem em laboratório.
Claro que não podemos terminar este texto sem citar que a Tabela Periódica também nos esclarece sobre as propriedades referentes aos elementos químicos. São elas:
- tamanho dos seus átomos;
- energia necessária para retirar um elétron de um átomo no estado gasoso;
- capacidade de atrair para perto de si os elétrons da ligação com outro átomo;
- energia liberada no estado gasoso ao receber um elétron;
- capacidade de liberar os elétrons da ligação com outro átomo;
- tendência de sofrer fusão ou ebulição; e
- capacidade que um átomo tem de reagir com outro, formando novas substâncias.
De toda a Tabela Periódica, o elemento fósforo foi o primeiro isolado em laboratório, há cerca de 350 anos. Desde então, a Tabela Periódica sofreu já várias alterações! A cada ano, mais e mais descobertas acontecem. Só em 2016, por exemplo, foram oficializados os elementos Tenessine, Nihonium, Moscovium e Oganesson. Também, nos últimos anos, foi incluído na Tabela o elemento 118. Então, o estudo da Tabela Periódica deve ser constante!
Veja Também: Cientista cria tabela periódica interativa que pode ser a solução dos seus problemas
PUBLICIDADE
CONTINUE LENDO ABAIXO
Fontes: Ecycle, UOL, Wikipedia.
Imagens: Todos os Créditos reservados aos respectivos proprietários (sem direitos autorais pretendidos). Caso eventualmente você se considere titular de direitos sobre algumas das imagens em questão, por favor entre em contato com contato@engenharia360.com para que possa ser atribuído o respectivo crédito ou providenciada a sua remoção, conforme o caso.
Comentários
Redação 360
Nossa missão é mostrar a presença das engenharias em nossas vidas e a transformação que promovem, com precisão técnica e clareza.

