Nosso cuidado diário com a saúde nos faz refletir sobre questões de limpeza, higiene e descontaminação em geral, bem como nossos hábitos relacionados a isso. Contudo, nessas horas, é comum surgir a seguinte dúvida: qual o tratamento dedicado à superfície ou à água é mais eficaz? Bem, antes disso, precisamos entender os conceitos por trás da desinfecção. Confira o artigo a seguir, do Engenharia 360! Vamos falar um pouco da química do cloro na inativação de microrganismos e o que isso tem a ver com engenharia.
O que é ‘cloro’ para a Engenharia?
O cloro é um agente desinfetante que utilizamos nos sistemas de abastecimento de água, visando manter um residual livre que seja capaz de inativar microrganismos que porventura contaminem a rede ou, por exemplo, nosso reservatório domiciliar (a caixa d’água). Nas soluções residenciais, estamos mais familiarizados com compostos que têm cloro, como hipoclorito de cálcio (comercializado em pastilhas e em geral usado para desinfetar piscinas) e hipoclorito de sódio, a água sanitária.
Considerando o cloro, portanto, como um insumo em uma estação de tratamento de água (ETA), sua demanda é uma questão de gerenciamento da planta e, portanto, de engenharia. Além disso, a maneira como será aplicado também determinará como a instalação será concebida.
A saber, as formas de aplicação seriam a injeção de cloro gasoso ou a geração no local por eletrólise, por exemplo.
O que é a cloração?
Usamos “cloração” como termo genérico para a adição de cloro à água, que pode ter objetivos como a desinfecção, ou seja, a inativação de microrganismos até um nível seguro para a saúde, ou a oxidação. No segundo caso, estamos nos referindo a alterações nas características da água por reações químicas de oxirredução. Ou seja, o cloro e seus compostos são fortes agentes oxidantes.
A característica oxidante implica em vários efeitos sobre microrganismos. Dentre eles, podemos citar a oxidação do protoplasma celular enquanto o composto é difundido na célula e, além disso, acredita-se que o cloro é capaz de alterar o arranjo de algumas enzimas e, em muitos casos, inativa-las diretamente.
PUBLICIDADE
CONTINUE LENDO ABAIXO
Outra questão é o “ataque”, isto é, a alta reatividade com elementos da membrana celular dos microrganismos, destruindo sua permeabilidade seletiva e, portanto, permitindo a difusão de solutos vitais para as células. Basicamente, os microrganismos são inativados diretamente ou tornam-se muito enfraquecidos e expostos às condições ambientais.
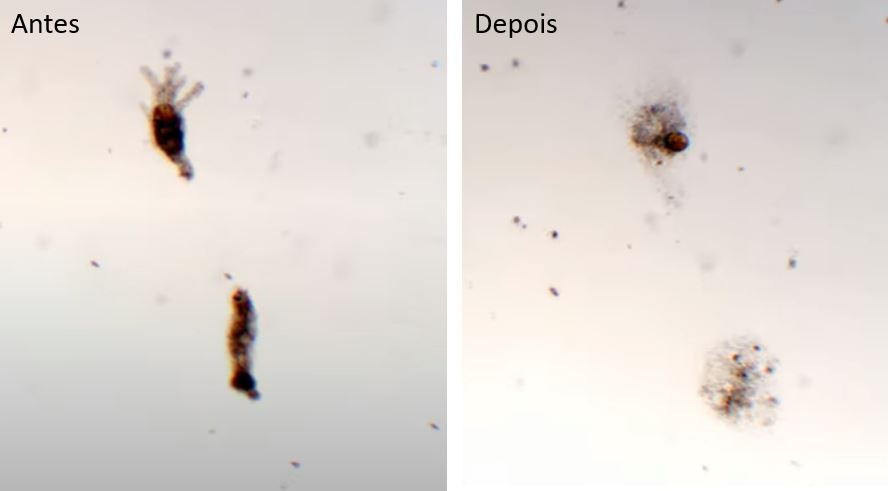
É importante destacar que microrganismos de diferentes espécies apresentam tolerâncias variadas ao desinfetante. Inclusive, que a inativação em si dependerá de uma relação entre a concentração de cloro disponível na água e o tempo de contato.
Como saber quanto cloro usar?
A demanda de cloro é função da qualidade da água. Entende-se que ao sair do sistema de tratamento convencional, a água estará livre de microrganismos patogênicos e outros compostos oxidáveis, então não haverá muito o que o cloro “atacar”. Entretanto, falando de química, há toda uma questão de equilíbrio que dependerá de fatores como pH e temperatura.
Outro detalhe é que para que o cloro aja de forma efetiva para inativar os microrganismos, é necessário um tempo de contato. Em casa, por exemplo, para alvejar roupas, a gente precisa deixa-las de molho por um tempo, não é? A inativação de microrganismos também não ocorre de forma instantânea.
PUBLICIDADE
CONTINUE LENDO ABAIXO
Quando o cloro é adicionado à água, várias espécies encontram-se em equilíbrio, dentre as quais o íon cloreto (Cl–) e o ácido hipocloroso (HOCl). A ação desinfetante e oxidante do cloro é controlada pelo ácido hipocloroso, um ácido fraco, que desejamos manter presente na água. Por isso o pH deve ser favorável à sua manutenção. As águas de abastecimento, em geral, apresentam valores de pH em que as formas presentes são o ácido hipocloroso (HOCl) e o íon hipoclorito (OCl–), formas que chamamos de cloro residual livre.
O objetivo é manter uma concentração adequada de cloro residual livre na água, sem comprometer a segurança dos usuários e seguindo o Padrão de Potabilidade do Ministério da Saúde. O residual livre, entretanto, não é apenas função de quanto é dosado, mas o nitrogênio amoniacal presente na água, pH, temperatura e tempo de reação. Mas o que esse nitrogênio tem a ver?
Cloração no breakpoint
Quando existem, na água, amônia e compostos amoniacais, ocorre a formação de compostos clorados ativos, denominados cloraminas. O cloro presente sob a forma de cloraminas é denominado cloro residual combinado. Essas substâncias são a monocloramina, dicloramina e tricloramina e sua formação será função de quantidade de nitrogênio presente, bem como pH, temperatura e o tempo de reação.
Existe ação desinfetante por parte das monocloraminas, mas a eficiência é menor do que a obtida pelo íon hipoclorito.
Dicloraminas e tricloraminas são desaconselháveis porque apresentam odor forte e baixo poder desinfetante. A destruição dessas moléculas pode ser obtida com o aumento da dosagem de cloro, gerando uma inflexão no gráfico que relaciona o cloro residual disponível com o dosado. Esse ponto é chamado de breakpoint e ele é conhecido por meio de testes em laboratório que usam a água a ser desinfetada, diferentes doses de cloro em um tempo fixo de contato e a análise do residual livre.
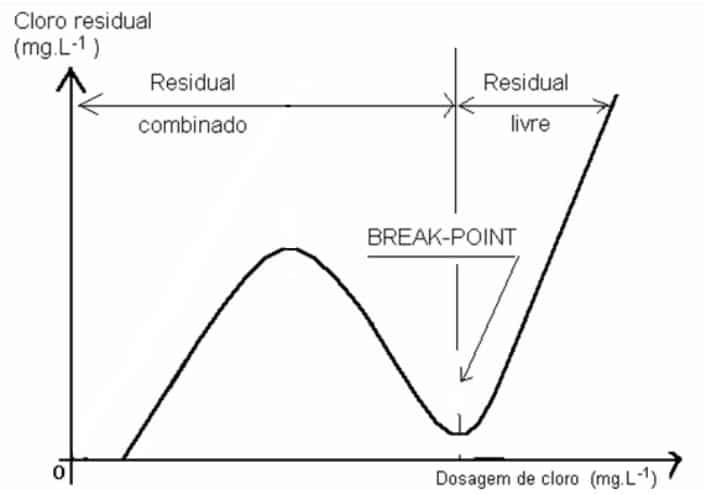
Vale apontar aqui que a desinfecção de esgoto tratado é uma prática ideal para evitar a contaminação do corpo d’água receptor. Essa matriz, diferentemente da água, está mais suscetível a apresentar níveis mais altos de nitrogênio amoniacal, exigindo, portanto, doses de cloro maiores para alcançar o breakpoint.
Referências:
DI BERNARDO, Luiz; DANTAS, Angela Di Bernardo; VOLTAN, Paulo Eduardo Nogueira. Métodos e técnicas de tratamento de água. São Carlos: Editora Cubo, 2017.
MACEDO, J. A. B.; Andrade, N. J.; Chaves, J. B. P.; Araújo, J. M. A.; Silva, M. T. C.; Jordão, C. P. Formação de trihalometanos em soluções sanificantes utilizadas no processo de desinfecção de industrias de alimentação. Revista do instituto de lacticinios Cândido Tostes, 54(309), 216-230, 1999.
MEYER, Sheila T.. O uso de cloro na desinfecção de águas, a formação de trihalometanos e os riscos potenciais à saúde pública. Cad. Saúde Pública, Rio de Janeiro , v. 10, n. 1, p. 99-110, mar. 1994 .
Imagens: Todos os Créditos reservados aos respectivos proprietários (sem direitos autorais pretendidos). Caso eventualmente você se considere titular de direitos sobre algumas das imagens em questão, por favor entre em contato com contato@engenharia360.com para que possa ser atribuído o respectivo crédito ou providenciada a sua remoção, conforme o caso.
Comentários

Kamila Jessie
Doutora em Hidráulica e Saneamento pela Universidade de São Paulo (EESC/USP) e Mestre em Ciências pela mesma instituição; é formada em Engenharia Ambiental e Sanitária pelo Centro Federal de Educação Tecnológica de Minas Gerais (CEFET-MG) com período sanduíche na University of Ottawa, no Canadá; possui experiência em tratamentos físico-químicos de água e efluentes; atualmente, integra o Centro de Pesquisa em Óptica e Fotônica (CePOF) do Instituto de Física de São Carlos (USP), onde realiza estágio pós-doutoral no Biophotonics Lab.


